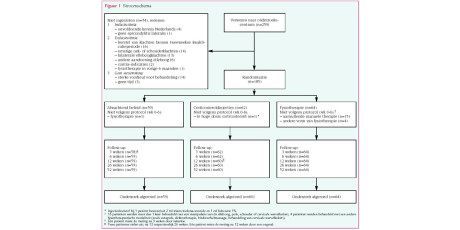
Kortekaas et al. geven in hun artikel een overzicht van huisartsgeneeskundige trials uit de afgelopen twintig jaar.1 Ze concluderen dat het jaarlijks aantal gepubliceerde RCT’s op het gebied van de huisartsgeneeskunde in die afgelopen jaren steeds gestegen is, maar dat bepaalde aandoeningen (psychiatrie en chronische aandoeningen) relatief zijn oververtegenwoordigd en dat andere terreinen (‘kleine kwalen’: dermatologie, KNO, oogheelkunde) juist relatief weinig aan bod zijn gekomen.
De onderzoekers geven in hun discussie aan dat zij vanwege beperkte middelen concessies hebben moeten doen aan de grondigheid van het overzicht. Dat zij bij controle achteraf 60% van de trials bleken te hebben gemist, geeft aan dat de zoekstrategie niet erg ‘sensitief’ is geweest. De auteurs concluderen dat ze geen aanwijzingen voor selectie hebben, maar geven verder niet aan hoe ze dat hebben onderzocht. Voor huisartsgeneeskundig onderzoekers geven hun conclusies en aanbevelingen echter voldoende stof tot nadenken.
Wordt het juiste onderzoek wel gedaan? De auteurs raden aan om naar de lacunebak van het Nederlands Huisartsen Genootschap (NHG) te kijken. Daarin zijn per NHG-Standaard de belangrijkste vragen samengebracht die open bleven na afronding van de standaard. Daar staan inderdaad interessante vragen bij waarvan je je afvraagt waarom we ze nog niet onderzocht hebben, zoals: ‘Wat is de optimale (medicamenteuze) behandeling van proctitis?’ uit de NHG-Standaard Rectaal bloedverlies.
Haken en ogen
Voor een huisartsgeneeskundige trial zijn middelen nodig (geld, materiaal, personeel), huisartsen en patiënten. En de trial moet uitvoerbaar zijn.2 Om bij dat laatste te beginnen: een huisarts moet allereerst de vraag relevant vinden en moet het vervolgens ook ethisch verantwoord vinden om alle behandelopties (gerandomiseerd) aan zijn patiënten aan te bieden, anders zal hij geen patiënt uitnodigen om mee te doen. Een voorbeeld: huidschimmel is een van de meest voorkomende aandoeningen in de praktijk, nader onderzoek zou dus een hoge prioriteit moeten hebben. De NHG-Standaard Dermatomycosen beschrijft een aantal lacunes, waaronder de drie in de [tabel]. Voor alle drie de te onderzoeken behandelingen zijn orale middelen de eerste keuze. Zou u als huisarts – of als vader, moeder of partner – een patiënt aanraden om ten behoeve van de kennisontwikkeling in de huisartsgeneeskunde mee te doen aan een trial waarin het gebruikelijke middel vergeleken wordt met de genoemde alternatieven? Voor de onderzoeker of huisarts zou het goed zijn om als gedachte-experiment een patiëntinformatiebrief op te stellen die eerlijk aangeeft wat het gangbare middel is en waarom de genoemde alternatieven nog onderzocht moeten worden. Dat is in dit geval niet gemakkelijk.
TabelLacunes in de NHG-Standaard DermatomycosenOpen tabel
| Onderwerp | Toelichting | Bron |
|---|---|---|
| Is een lokaal antimycoticum in combinatie met ureumcrème een effectieve behandeling voor voetschimmel met mocassinpatroon? | Wij hebben enkele kleine onderzoeken van matige kwaliteit gevonden over de behandeling van voetschimmel met mocassinpatroon met een lokaal antimycoticum en ureumcrème. Er was te weinig evidence om hier een uitspraak over te doen. | Noot 17 |
| Is miconazol in applicatievloeistof een effectieve behandeling voor een onychomycose? | Voor de lokale behandeling van onychomycosen is er in diverse landen amorolfine en ciclopiroxnagellak in de handel. In Nederland is enkel miconazol in applicatievloeistof beschikbaar, maar er zijn geen goede onderzoeken bekend over effectiviteit van dit middel. | Noot 20 |
| Is het effectief om ter verspreiding van tinea capitis een lokale behandeling met antimycotica te adviseren? | Dit wordt in de literatuur of in enkele richtlijnen geadviseerd, maar het is onduidelijk of het effectief is. | Noot 24 |
Een ander probleem is dat het contrast in de trial wel gehandhaafd moet kunnen worden. In dezelfde standaard staat de vraag: ‘Hoe effectief zijn niet-medicamenteuze adviezen zoals het vermijden van factoren die maceratie van de huid bevorderen, dragen van katoenen ondergoed/sokken/kleding en het dragen van badslippers?’ Hoe zouden we dat gerandomiseerd kunnen uitzetten? Patiënten die van zichzelf al katoenen sokken dragen, vragen deze een maand lang te ruilen voor synthetische? Alleen patiënten met synthetische sokken in de trial opnemen? Alleen patiënten met manifeste zweetvoeten? Hoe vaak moeten de sokken worden gewisseld? Contrast: open schoenen met katoenen sokken, dichte schoenen met katoenen sokken, open schoenen met synthetische sokken, dichte schoenen met synthetische sokken? Hoe controleren we de compliantie? Dit wordt geen eenvoudige trial!
Alledaags is uit
Ik stel voor om een commissie van huisarts-onderzoekers nog eens door de lacunebak heen te laten gaan om de onderzoekbaarheid van de lacunes te beoordelen. Het zou voor de huisartsgeneeskunde goed zijn als uit de onderzoekbare vragen er jaarlijks bijvoorbeeld tien worden geprioriteerd die dan ook extra aandacht en hopelijk ook middelen krijgen.
Waar moeten die middelen vandaan komen? Het programma Alledaagse ziekten van ZonMw is stopgezet, het Doelmatigheidsprogramma van ZonMw lijkt zich meer en meer te beperken tot aandoeningsgebieden die op nationaal niveau ‘groots en meeslepend’ (lees: duur) zijn. Daar maken anusjeuk of proctitis geen kans meer… Toch zijn er nog mogelijkheden. Veel afdelingen hebben assistenten in opleiding tot huisarts en onderzoeker (aiotho’s), die gedeeltelijk uit eigen middelen of door het opleidingsfonds SBOH worden betaald. Mogelijk komt daar binnenkort nog geld bij in het kader van de verdere ‘academisering’ van de opleiding, waarover de afdelingen momenteel met de SBOH praten. Is het een idee om de top tien van lacunes te betrekken bij de keuze van onderwerpen voor deze gelden?
Waarschijnlijk zal de incidentie of prevalentie van de aandoening een belangrijk criterium zijn voor de prioritering. Wat is nou leuker en leerzamer dan de aios (dus niet alleen de aiotho’s) in het kader van de academisering een rol te geven bij het rekruteren en begeleiden van patiënten in de hieruit voortkomende trials? Ze zouden een rol kunnen spelen bij de gegevensverzameling: als die geblindeerd moet gebeuren, kan dat in een andere dan de eigen praktijk. Met het omvangrijke netwerk van opleidingspraktijken en het grote aantal aios per opleiding moet een infrastructuur te maken zijn die geschikt is voor onderzoek naar veel voorkomende aandoeningen. De opbrengst is kennisontwikkeling voor het vak, hulp voor een collega-aios (de aiotho) en ervaring met het doen van onderzoek (een van de competenties).
Alternatieve designs
De NHG-Standaarden dekken een groot deel van het huisartsgeneeskundig handelen. De lacunes zouden we op de hier beschreven manier systematisch kunnen opvullen. Zijn we er dan? Ik vrees van niet. Trials zijn vooral geschikt om voor één aandoening diverse, scherp gecontroleerde interventies te vergelijken. Mijns inziens liggen de grote uitdagingen voor de huisartsgeneeskunde de komende jaren niet zozeer in interventies bij geïsoleerde aandoeningen als wel in complexere vraagstukken, zoals de zorg voor kwetsbare ouderen, multimorbiditeit, preventie, praktijkvoering, taakdelegatie, ketenzorg en ict-toepassingen. Deze onderwerpen laten zich moeilijk in gerandomiseerde trials vangen.3 We zullen dus naast trials waarin patiënten worden gerandomiseerd ook moeten nadenken over alternatieve designs, die meer ruimte geven aan de complexiteit van het vraagstuk en de veranderbaarheid van de omgeving. Steeds vaker zullen praktijken, zorggroepen en andere samenwerkingsverbanden in zogeheten clustergerandomiseerde trials de eenheid van randomisatie worden. Dat stelt weer specifieke methodologische uitdagingen, zoals het definiëren en beschrijven van de verschillende interventies.4 Steeds vaker wordt bij evaluatie van organisatieveranderingen het stepped-wedge design gebruikt.5 Het voordeel van deze opzet is dat alle deelnemende organisatieonderdelen (bijvoorbeeld praktijken of zorggroepen) de nieuwe manier van werken overnemen, maar dat de onderzoekers het tijdstip waarop dat gebeurt randomiseren [figuur]. Ieder van de clusters levert dan metingen over de periode vóór en de periode ná de interventie of organisatieverandering. Voor elke cluster is de lengte van beide periodes verschillend en de verdeling tussen pre en post wordt gerandomiseerd toegekend.
Tot slot
Er zullen nog veel huisartsgeneeskundige trials nodig zijn om onze effectiviteitsvragen in de praktijk te kunnen beantwoorden. We moeten in de huisartsgeneeskunde ook onder ogen zien dat je niet alles gerandomiseerd kunt onderzoeken. Soms simpelweg omdat een van de behandelopties al te zeer in de praktijk is ingeburgerd, maar steeds vaker ook omdat de onderzoeksvraag te complex is voor een trial op patiëntniveau.
Zoals Kortekaas et al. in hun artikel al aangeven, slaat Nederland zeker geen slecht figuur als het gaat om de totale onderzoeksoutput en de return on investment van onderzoeksgeld. Dat is voor een groot deel te danken aan de medewerking van duizenden huisartsen aan onderzoek en we mogen er best trots op zijn. Ik hoop dat we als Nederland en als huisartsen ook de komende jaren in de top van de wereld blijven staan!
Literatuur
- 1.↲Kortekaas MF, Meijer A, Van de Pol AC, De Wit NJ. RCT’s in de huisartsgeneeskunde, 1990-2010. Huisarts Wet 2012;55:486-91.
- 2.↲Bakkenist T, Assendelft P, Van Geldrop W. Wetenschappelijk onderzoek in de huisartsenpraktijk. Wie doet er mee? Huisarts Wet 2003;46:181-5.
- 3.↲Hordijk M. Klinische trial krijgt concurrentie. Med Contact 2011;66:2045-7.
- 4.↲Smelt AF, Van der Weele GM, Blom JW, Gussekloo J, Assendelft WJ. How usual is usual care in pragmatic intervention studies in primary care? An overview of recent trials. Br J Gen Pract 2010;60:e305-18.
- 5.↲Dekkers OM. Het ‘stepped wedge’-design. Ned Tijdschr Geneeskd 2012;156:A4069.
- 6.↲Lucassen PLBJ, Olde Hartman TC, Mazel JA. Kwalitatief onderzoek: Praktische methoden voor de medische praktijk. Houten: Bohn Stafleu van Loghum, 2007.
Reacties
Er zijn nog geen reacties.