Samenvatting
De Vries MP, Van den Bemt L, Aretz K, Thoonen BPA, Muris JWM, Kester A, Cloosterman S, Van Schayck CP. Helpen huisstofmijtwerende hoezen? Huisarts Wet 2008;51(1):12-7. Achtergrond De effectiviteit van huisstofmijt (HSM) werende hoezen is nog steeds onderwerp van discussie. Doel Onderzoeken of de combinatie van HSM-werende hoezen en zelfbehandeling, gebaseerd op piekstroomwaarden en symptomen, leidt tot gebruik van minder inhalatiecorticosteroïden (ICS) in vergelijking met zelfbehandeling alleen. Opzet Prospectief, gerandomiseerd, dubbelblind, placebogecontroleerd onderzoek. Methoden We includeerden astmapatiënten van zestien tot zestig jaar, die een een allergie hadden voor HSM, en ICS gebruikten. We legden ze uit hoe ze het zelfbehandelplan moesten gebruiken op basis van piekstroomwaarden en symptomen. Na een oefenperiode van drie maanden startte de interventieperiode van twee jaar met HSM-ondoorlaatbare of placebo hoezen. De primaire uitkomstmaat was gebruik van ICS, daarnaast keken we ook naar piekstroomparameters, astmacontrole en symptomen. Resultaten Er begonnen 126 patiënten aan de interventieperiode met de hoezen. Na een en twee jaar was er een significant verschil in blootstelling aan allergenen tussen de groep met HSM-werende hoezen en de placebogroep (p 0,001). We vonden geen significant verschil tussen de groepen in gebruik van ICS (p = 0,08), ochtend piekstroomwaarde (p = 0,52), piekstroomvariabiliteit (p = 0,36), dyspnoe (p = 0,46), piepen (p = 0,77) en hoesten (p = 0,41). Er was ook geen verschil in astmacontrole tussen de interventie- en controlegroep. Conclusie HSM-werende hoezen in combinatie met zelfbehandeling leiden niet tot minder gebruik van ICS dan zelfbehandeling alleen.
Inleiding
Inflammatie is het onderliggende pathofysiologische mechanisme bij astma en dit leidt tot een variabele beperking in de luchtstroom, wat zorgt voor klachten. 1 Inhalatiecorticosteroïden (ICS) bestrijden de inflammatie en vormen daarom de hoeksteen in de behandeling van astma. 2-5 Vanwege mogelijke bijwerkingen van ICS is het van belang om de dosering zo laag mogelijk te houden. 6 Bij patiënten met mild astma is het vaak mogelijk om de dosering te verminderen. 78 Zelfbehandelplannen zijn geschikt om de dosering van ICS naar een optimaal niveau te brengen en te houden. Daarnaast is aangetoond dat zelfbehandelplannen positieve effecten hebben op diverse astmagerelateerde uitkomstmaten. 891011 Vooral geïndividualiseerde geschreven actieplannen geven steeds een positief effect op astmagerelateerde uitkomstmaten omdat ze gebaseerd zijn op de persoonlijk beste piekstroomwaarde, gebruikmaken van actiepunten en gebruiksaanwijzingen geven voor zowel inhalatie als orale steroïden om vroege exacerbaties te behandelen. 12 Allergeenvermijding maakt vaak onderdeel uit van een zelfbehandelplan, maar het is nog niet bekend of het een effectief onderdeel is. Het onderzoek van Thoonen et al. heeft aangetoond dat zelfbehandeling een significante reductie van ICS oplevert in vergelijking met de gebruikelijke zorg. 8 Verder bleek in dit onderzoek dat de zelfbehandelingsgroep significant hogere kosten maakte voor HSM allergeenvermijdende maatregelen in vergelijking met de usual-caregroep. 13 Het is niet duidelijk of deze maatregelen bijdroegen aan het positieve effect van de zelfbehandeling. Het is niet zinvol om astma alleen te behandelen met inhalatiecorticosteroïden, omdat men de oorzaak van de inflammatie dan niet behandelt. Bij de meeste astmapatiënten draagt blootstelling aan prikkels bij aan het inflammatie proces. Blootstelling aan prikkels als HSM-allergenen kan inflammatie veroorzaken en in stand houden. 1415 Matrashoezen, dekbedhoezen en kussenhoezen zijn de effectiefste methode om de blootstelling aan HSM allergenen te reduceren. 1617181920 Maar de effecten van HSM ondoorlaatbare hoezen op klinische parameters zijn onderwerp van discussie. 17,20-27 Dit onderzoek bekijkt of HSM allergeenvermijding met hoezen een toegevoegde waarde heeft bij de zelfbehandeling, en of dit leidt tot gebruik van minder ICS en betere astmacontrole in vergelijking met zelfbehandeling alleen.
Methoden
Patiëntselectie
We rekruteerden astmapatiënten uit Brabant en Limburg via huisartsenpraktijken en een open werving met advertenties in de lokale pers. Patiënten die wilden deelnemen, screenden we op in- en exclusie criteria. Inclusiecriteria waren: leeftijd van 16 tot 60 jaar, diagnose astma, allergie voor HSM en gebruik van ICS, gedefinieerd volgens de NHG-Standaard Astma bij Volwassenen: Behandeling. 28 Allergie bepaalden we aan de hand van een Phadiatop ® voor inhalatieallergenen. Indien positief voerden we radio-allergo-sorbent tests (RASTs) uit op specifiek IgE voor graspollen, boompollen, HSM, kat en hond. IgE-waarden boven 0,35 kU/l (klasse 1 of hoger) werden beschouwd als positief (klasse 1 tot en met 3 milde, klasse 4 tot en met 6 ernstige allergie). Exclusiecriteria waren: ernstige aandoeningen met een lage overlevingskans, andere aandoeningen die de longfunctie beïnvloeden of bronchiale klachten geven, gebruik van orale steroïden of inhalatie cromoglycaten, reeds gebruiken van huisstofmijtwerende matrashoezen en allergie voor kat of hond, terwijl dit dier aanwezig is in huishouden. De lokale Medisch Ethische Toetsingscommissie keurde het onderzoek goed. Alle patiënten verleenden toestemming voor deelname door schriftelijk informed consent.
Onderzoeksopzet
Dit onderzoek was een prospectief, dubbelblind, placebogecontroleerde klinische trial met een run-inperiode van drie maanden, gevolgd door een interventie periode van twee jaar. Patiënten werden at random toegewezen aan de interventie-of controlegroep. De interventiegroep kreeg actieve allergeen vermijdende maatregelen, bestaande uit non-polyurethane vochtdoorlatende, HSM-ondoorlaatbare hoezen voor matras, dekbed en kussen. De controlegroep kreeg HSM-doorlaatbare hoezen. Alle hoezen werden geleverd door één leverancier en waren niet van elkaar te onderscheiden. Patiënten kregen geen voorlichting over andere methoden van HSM-allergeenvermijding.
Zelfbehandeling
We leerden patiënten om het zelfbehandelplan te gebruiken en om de dosis ICS aan te passen op geleide van symptomen en piekstroomwaarden tijdens een run-inperiode. Huisartsen en speciaal getrainde onderzoeksverpleegkundigen gaven de instructies volgens een gestandaardiseerde methode. Piekstroom werd gemeten met een draagbare piekstroommeter (Asmaplan+, Vitalograph ®, Buckingham, UK). De meeste deelnemers aan het onderzoek gebruikten budesonide 200 microg in Turbuhaler ®. We berekenden dosis equivalenten voor verschillende inhalatiecorticosteroïden en toedieningsvormen. Voor de berekening verdubbelden we de dosering van dosisaërosolen om vergelijkbare doseringen met poederinhalatoren te krijgen. 29 Thoonen et al. hebben eerder de details van het zelfbehandelplan beschreven. 8 In het kader staat een samenvatting van het zelfbehandelplan. De patiënten noteerden gegevens over symptomen, ochtend- en avondpiekstroom en medicatiegebruik (ICS, luchtwegverwijders en overige medicatie) elke week in dagboekjes. Na een oefenperiode van drie maanden ging de interventieperiode van start met de placebogecontroleerde allergeenvermijding en een follow-upduur van twee jaar. Gedurende de run-in periode werden patiënten getraind in gebruik van de zelfbehandeling. In drie bezoeken leerden zij hoe ze de dagboekjes moesten invullen, hoe de piekstroommeter gebruikt moest worden en hoe ze stapsgewijs de medicatie konden aanpassen. Drie maanden later ging de interventieperiode van start. Tijdens de interventieperiode vond er elke zes maanden een huisbezoek plaats om de uitvoer van het zelfbehandelplan te controleren.
Kader Samenvatting van zelfbehandelplan
Instructies voor ophogen
-
Als piekstroom (PS) verslechtert tot < 80% PS ≥ 60% van persoonlijk beste waarde (PBW) in 2 van de 3 opeenvolgende dagen:
- verdubbel dosering budesonide;
- indien onvoldoende respons binnen 3 weken: verdubbel dosering budesonide weer.
-
Als piekstroom verslechtert tot < 60% PS ≥ 40% van PBW in 2 van de 3 opeenvolgende dagen:
- verhoog dosering budesonide tot 800 microg 2 maal daags;
- in geval van onvoldoende respons binnen 2 dagen: neem contact op met de huisarts.
- Als piekstroom verslechtert tot < 40% of PBW: neem direct contact op met de huisarts om een stootkuur prednison te starten.
Instructies voor verlagen
- Als piekstroom verbetert tot ≥ 40% PS < 60% van PBW: continueer huidige dosering budesonide totdat de PS >80% is van PBW.
- Als piekstroom verbetert tot ≥ 60% PS < 80% PBW: continueer huidige dosering budesonide totdat de PS >80% is van PBW.
- Als piekstroom verbetert tot ≥ 80% van PBW: halveer dosering budesonide wanneer de PS ≥ 80% gedurende 6 weken.
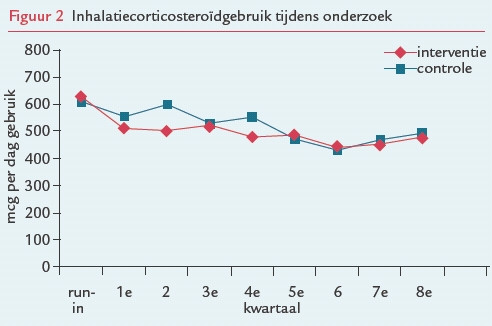
Resultaten
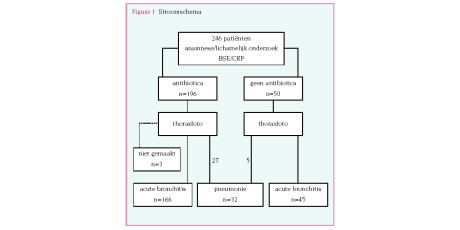
We selecteerden de patiënten via huisartsenpraktijken en via open werving. Figuur 1 geeft de patiëntenstroom weer ten tijde van selectie, inclusie en gedurende onderzoek. De werving van patiënten vond plaats tussen september 1999 en december 2001. In juli 2004 was de dataverzameling klaar.
| Interventie | Controle | |
| Aantal patiënten | 63 | 63 |
| Leeftijd in jaar (SD)* | 39,8 (13,2) | 43,9 (11,7) |
| Geslacht M/V | 32/31 | 41/22 |
| Gemiddelde FEV %-voorspeld bij inclusie (SD) | 86,5 (16,1) | 89,1 (14,6) |
| Gemiddelde FEV %-voorspeld bij start interventie (SD) | 85,0 (17,7) | 85,4 (14,7) |
| Gemiddelde dosis ICS bij inclusie (SD), in microg per dag | 656 (448) | 657 (474) |
| Gemiddelde dosis ICS bij start interventie (SD), in microg per dag | 519 (441) | 532 (420) |
| 3
9 21 20 2 4 4 | 7
11 22 20 - 3 - | |
| Gemiddeld aantal overige allergieën (SD) | 2,0 (1,4) | 1,6 (1,6) |
| Roken: | 44
16 3 | 32
25 6 |
| Gebruik langwerkende beta-2-agonisten | 15 | 9 |
Reacties
Er zijn nog geen reacties.