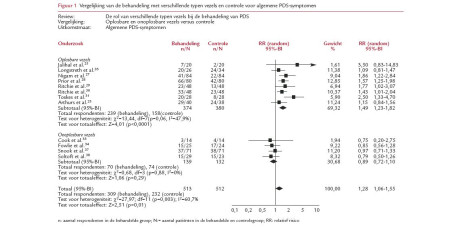
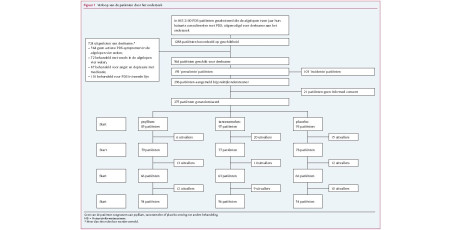
Samenvatting
In deze beschouwing worden aanbevelingen gegeven voor de diagnostiek en behandeling van PDS-patiënten. Huisartsen kunnen PDS-patiënten op basis van de symptomen met zekerheid identificeren. Bij alarmsymptomen is aanvullend onderzoek geïndiceerd. De diagnose PDS wordt in de huisartsenpraktijk tevens bepaald door het ‘patiëntenprofiel’. De karakteristieken daarvan zijn: een frequent consultatiepatroon, een verhoogde prevalentie van somatische en psychiatrische comorbiditeit en een voorgeschiedenis met lichamelijk onverklaarde klachten. De huisarts zou de behandeling moeten starten met het onderzoeken van de perceptie en verwachtingen van de patiënt. De volgende stap is het geven van uitleg en geruststelling, waarbij de goedaardige achtergrond van het syndroom wordt uitgelegd. Leefstijlaanpassing is onderdeel van de behandeling. PDS-patiënten met functionele of psychiatrische comorbiditeit hebben mogelijk baat bij psychologische interventies of medicamenteuze behandeling.
De kern
- Zowel huisartsen als patiënten beschouwen buikpijn en een opgeblazen gevoel als de belangrijkste symptomen van PDS.
- De ernst van de klachten - en niet de impact op de kwaliteit van leven of de ervaren stress - bepaalt of de patiënt met PDS de huisarts frequent consulteert.
- PDS is geassocieerd met een hoge prevalentie van comorbiditeit. De prevalentie van somatische comorbiditeit neemt af na de diagnose, terwijl de prevalentie van functionele en psychiatrische comorbiditeit hoog blijven.
Inleiding
Het prikkelbaredarmsyndroom (PDS) is een functionele aandoening met een afwijkend ontlastingspatroon of met kenmerken van een verstoorde stoelgang.1 PDS-patiënten consulteren de huisarts veelvuldig, zowel voor PDS als voor andere problemen. Hoewel veel pathosfysiologische verklaringen voor PDS zijn aangedragen, is de etiologie nog steeds onbekend. Het lijkt erop dat dezelfde mechanismen verantwoordelijk zijn voor buikpijn en een afwijkend ontlastingspatroon bij mensen met en zonder PDS. PDS kan het beste worden verklaard met het bio-psychosociale model.2345 De behandeling van PDS dient te zijn gebaseerd op de aard en ernst van de symptomen, de mate van psychologische ontregeling en de eventuele functionele beperkingen.
Diagnostiek: symptomen en het patiëntenprofiel
Zoals bij veel functionele aandoeningen zal de huisarts bij het diagnosticeren van PDS balanceren tussen een symptoomdiagnose en het uitsluiten van andere gastro-intestinale aandoeningen. De huisarts is de eerst aanwezen specialist die met deze uitdaging wordt geconfronteerd en ook degene die de toon zet. Diverse factoren beïnvloeden deze balans: de kans op organische ziekte, de aanwezigheid van alarmsymptomen, de noodzaak om somatisatie te voorkomen, de aanwezigheid van comorbiditeit en psychosociale factoren, en de behoefte van dokter of patiënt aan diagnostische zekerheid. Huisartsen en patiënten beschouwen beiden buikpijn en een opgeblazen gevoel als predominante symptomen van PDS.6 Huisartsen hanteren andere criteria dan specialisten in de tweede lijn, die uitgaan van de strikte, op consensus gebaseerde criteria.78 In ons onderzoek voldeed slechts eenderde van de door de huisarts gediagnosticeerde patiënten aan de strikte Rome-definitie van meer dan drie maanden buikpijn in het voorgaande jaar.69 Huisartsen zijn duidelijk in staat PDS-patiënten met zekerheid te identificeren, maar hoe stellen ze de diagnose in de dagelijkse praktijk? Algemene symptomen, zoals buikpijn of een opgeblazen gevoel, leiden tot de diagnose. Aanvullende symptomen, zoals obstipatie, diarree, winderigheid of dyspepsie, kunnen de diagnose ondersteunen. De predominante PDS-symptomen kunnen per cultuur verschillen.10 Het gegeven dat huisartsen geen strikte tijdslijn gebruiken, is blijkbaar een van de belangrijkste verschillen met het diagnostische proces zoals dat is gesuggereerd door de Rome-groep. Waar de Rome-criteria de aanwezigheid van de symptomen gedurende minstens een jaar noodzakelijk achten, diagnosticeren huisartsen PDS bij patiënten met een veel kortere ziektegeschiedenis. Recentelijk verschenen richtlijnen gaan uit van een in de huisartsenpraktijk toepasbare definitie van PDS inclusief buikpijn of ongemak, opgeblazen gevoel en verandering in het ontlastingpatroon gedurende minimaal vier weken.10 De diagnose in de huisartsenpraktijk wordt ook bepaald door het ‘patiëntenprofiel’. Vrouwen hebben vaker PDS en er zijn familiepatronen van PDS door de generaties heen te herkennen. Enkele karakteristieken ondersteunen dit ‘PDS-profiel’: een frequent consultatiepatroon, een recent ingrijpend life event, verhoogde prevalentie van somatische en psychiatrische comorbiditeit, en een voorgeschiedenis met lichamelijk onverklaarde klachten. Een van de essentiële verschillen tussen het diagnostisch proces in de eerste en tweede lijn is dat huisartsen – dankzij de langdurige relatie met de patiënt – op de hoogte zijn van de karakteristieken van dit patiëntenprofiel.
De helft van de PDS-patiënten die de huisarts consulteren, bezochten het spreekuur meer dan eens in het voorgaande jaar.9 Vermindering van ziektespecifieke kwaliteit van leven en psychiatrische comorbiditeit of psychologische ontregeling zijn geassocieerd met consultatiegedrag. Maar deze aspecten speelden geen rol meer na correctie voor factoren die gerelateerd zijn aan de te onderzoeken risicofactoren en aan de uitkomst (confounding). Hoewel er aanwijzingen zijn dat psychiatrische comorbiditeit geassocieerd is met een toegenomen consultatiefrequentie bij patiënten met PDS, konden wij dit in ons onderzoek niet bevestigen.11121314 Van der Horst et al. toonden aan dat huisartspatiënten met PDS hun buikklachten vaker toeschreven aan factoren als stress en eetgewoonten, terwijl verwezen patiënten hun klachten relateerden aan een organische verklaring.15 Dit kan betekenen dat ervaren stress bijdraagt aan angst, depressie en somatisatie bij PDS-patiënten. Somatisatie bleek niet voorspellend voor het aantal consulten, maar huisartsen kunnen somatisatie mogelijk wel beïnvloeden door het inzetten van doelmatige diagnostiek en beleid en door aandacht te besteden aan het omgaan met de vaak langdurige klachten.161718 PDS is geassocieerd met veel comorbiditeit. In ons onderzoek in de huisartsenpraktijk bleek de kans op een comorbide functionele aandoening het meest vergroot bij PDS-patiënten vergeleken met gematchte controlegroepen.9 Somatische aandoeningen kwamen vaak voor bij patiënten met een korte historie van PDS (minder dan twee jaar), met een zesvoudige piek in het jaar dat de diagnose werd gesteld. De prevalentie van functionele, psychiatrische en psychosociale problemen verdubbelde in het jaar van de PDS-diagnose en bleef op dat niveau in de jaren daarna.9 De hoge prevalentie van functionele comorbiditeit bij PDS-patiënten duidt mogelijk op een somatisatiestoornis die zich als verschillende functionele syndromen presenteert. Whitehead suggereerde dat een hoge prevalentie van comorbiditeit patiënten met predominante psychologische genese onderscheidt van patiënten met een oorspronkelijke somatische verklaring.19 Onze resultaten bevestigen een toegenomen prevalentie van comorbiditeit ten tijde van de diagnose, maar gedurende de follow-up bleef alleen de prevalentie van psychologische comorbiditeit verhoogd.
De rol van aanvullend onderzoek
In de huidige richtlijnen is aanvullend onderzoek alleen aanbevolen in geval van alarmsymptomen (gewichtsverlies, rectaal bloedverlies, nachtelijke buikpijn of anemie), een gebrekkige therapeutische respons en aanhoudende diarree.20 De meeste huisartsen vinden dat PDS een positieve diagnose zou moeten zijn en zij vragen alleen bij alarmsymptomen aanvullend onderzoek aan. Daarentegen wil de helft van de patiënten aanvullend onderzoek of verwijzing naar de specialist.6 Dit verschil tussen de verwachting van de patiënt en de aanpak van de huisarts kan een optimale behandeling in de weg staan. In de dagelijkse huisartsenpraktijk wordt bij 15% van de PDS-patiënten aanvullend onderzoek verricht: 5% op de praktijk en 10% met een endoscopie.21 Uit onderzoeken is gebleken dat een intensieve diagnostiek bij verwezen patiënten van beperkte waarde is voor het aantonen van een organische verklaring. Laboratoriumonderzoek toonde schildklierstoornissen aan in 6% van de gevallen, terwijl routine-endoscopie in slechts 2% van de gevallen afwijkingen aantoonde.22 PDS is een chronische aandoening, waarbij 88% van de patiënten na 8 jaar follow-up nog steeds symptomen vertoont.23 Bij slechts een klein aantal van de in de huisartsenpraktijk gediagnosticeerde patiënten wordt een organische verklaring gevonden. Tot nu toe zijn routineonderzoeken naar colorectaal carcinoom, coeliakie of andere mogelijke organische diagnosen niet kosteneffectief gebleken.8 Deze observaties ondersteunen de aanbeveling om aanvullend onderzoek te beperken en de diagnostiek in eerste instantie te baseren op PDS-symptomen en aanvullende patiëntenkarakteristieken. Alleen bij patiënten met diarree is er mogelijk noodzaak voor aanvullend onderzoek om PDS van inflammatory bowel disorder te onderscheiden. Tot op heden wordt dit voornamelijk gedaan door endoscopie, maar in de nabije toekomst kunnen tests op fecale biomarkers, zoals calprotetine en lactoferrine, worden gebruikt om patiënten te selecteren voor endoscopie.24
Behandeling van PDS; welke weg te gaan?
De meerderheid (90%) van de patiënten met PDS wordt behandeld in de huisartsenpraktijk en gegeven het lage aantal verwijzingen lijkt dit ook de voorkeur te hebben.25 Succesvolle behandeling hangt vooral af van een zekere diagnose en een open en sterke dokter-patiëntrelatie. De behandeling begint met het onderzoeken van de perceptie en verwachtingen van de patiënt. Het geven van voorlichting en geruststelling is de volgende stap, met uitleg over de pathofysiologie en de symptomen van PDS, alsmede de prognose en de goedaardige achtergrond van het syndroom. Ten slotte komen de therapeutische mogelijkheden aan de orde, waarbij aandacht wordt besteed aan de beperkte resultaten van de huidige medicamenteuze behandeling en de noodzaak voor leefstijlaanpassing. Onderdeel daarvan is een dieetadvies, met nadruk op de toevoeging van vezels aan de voeding. In de helft van de gevallen start de behandeling van PDS in de huisartsenpraktijk met farmacotherapie.6 De meerderheid van de patiënten (67%) gebruikt volumevergrotende laxantia, bijvoorbeeld de oplosbare vezel psyllium.26 Oplosbare vezel biedt voordelen voor patiënten met PDS, terwijl onoplosbare vezel (tarwezemelen) terughoudend moet worden geadviseerd.
Psychologische interventies: de ultieme remedie?
Het omgaan met buikklachten is voor de meeste PDS-patiënten een groot probleem. Door verscheidende factoren mislukken copingstrategieën: ingrijpende life events, aanvullende somatische klachten, catastrofale gedachten (‘tekenen van pijn verpesten mijn dag’), overmatige zorgen, refractaire symptomen en een overmatige beperking van het dagelijkse functioneren. Het rationaliseren van de ziekteperceptie, het inzetten van copingstrategieën en het verminderen van stress en zorgen zijn effectieve methoden om de impact van PDS op het dagelijks leven te verminderen.27 Cognitief gedragstherapie (CGT), interpersoonlijke psychotherapie, hypnose en ontspanningsoefeningen kunnen mogelijk de symptomen verlichten en de kwaliteit van leven verbeteren.2829 ‘Mogelijk’, omdat de methodologie van de meeste onderzoeken suboptimaal is en de duurzaamheid van de effecten onbekend.30 De keuze voor een psychologische behandeling is voor iedere patiënt afhankelijk van zijn achtergrond en voorkeur, de beschikbaarheid en de kosten. Op dit moment is de beschikbaarheid van methoden en van geschoolde therapeuten beperkt. Psychologische interventies door verpleegkundigen/praktijkondersteuners, zoals problem solving treatment en CGT, kunnen bijdragen aan een bredere implementatie in de huisartsenpraktijk.
Samenvattend; een optimale benadering van PDS
PDS kan adequaat worden gediagnosticeerd in de huisartsenpraktijk, voornamelijk op basis van alleen de symptomen en het patiëntenprofiel. Aanvullend diagnostisch onderzoek om organische buikaandoeningen uit te sluiten, bijvoorbeeld endoscopie, is slechts nodig bij patiënten met alarmerende of aanhoudende symptomen. Voorlichting is van belang om zeker te stellen dat de ziekteperceptie van de patiënt rationeel is en overeenkomt met die van de huisarts.
Reacties
Er zijn nog geen reacties.