Samenvatting
Röder E, Berger MY, Hop WCJ, Bernsen RMD, De Groot H, Gerth van Wijk R. Sublinguale immunotherapie met graspollen is niet effectief bij jongeren met hooikoorts. Huisarts Wet 2007;50(12):586-92. Inleiding Sublinguale immunotherapie (SLIT) wordt beschouwd als een veiligere en gebruikersvriendelijkere methode dan subcutane immunotherapie. Daarom lijkt SLIT vooral geschikt voor de behandeling van kinderen en voor toepassing in de huisartsenpraktijk. Effectiviteitsonderzoeken bij kinderen hadden echter onvoldoende zeggingskracht om een uitspraak te doen over de effectiviteit van SLIT, en werden uitgevoerd bij kinderen die waren doorverwezen. Doel Het onderzoeken van de effectiviteit van SLIT bij kinderen bekend met een graspollenallergie bij de huisarts. Methoden Kinderen van 6-18 jaar met hooikoorts werden via de huisarts geïncludeerd en kregen gedurende 2 jaar gerandomiseerd placebo of graspollen SLIT voorgeschreven. In het hooikoortsseizoen scoorden de kinderen dagelijks de ernst van 5 symptomen – niezen, jeukende neus, waterige loopneus, neusobstructie en jeukende ogen – op een schaal van 0 tot 3. De primaire uitkomst was de gemiddelde dagelijkse totale symptoomscore (schaal 0-15) in de maanden mei-augustus van het tweede behandeljaar. Resultaten Van de 204 gerandomiseerde kinderen hebben we 168 kinderen ingesloten in de intention-to-treatanalyse (91 verum, 77 placebo). De gemiddelde dagelijkse totale symptoomscore van patiënten in de verumgroep en patiënten in de placebogroep was gelijk (verschil verum minus placebo: –0,08, 95%-BI -0,66 - 0,50; p = 0,78). We vonden geen verschillen tussen de groepen wat betreft dagen zonder symptoommedicatie, ziektespecifieke kwaliteit van leven, en algemene indruk van behandeleffect. Lokale bijwerkingen kwamen meer voor in de verumgroep (39% versus 17% van de deelnemers; p = 0,001). Conclusie Sublinguale immunotherapie met graspollen is niet effectief bij kinderen die met hooikoorts bij de huisarts komen. Op dit moment kan SLIT niet worden aanbevolen als behandeling voor jongeren met een graspollenallergie.
Wat is bekend?
- Kinderen met hooikoorts hebben tijdens het pollenseizoen een verminderde kwaliteit van leven.
- Subcutane immunotherapie vermindert klachten van rhinoconjunctivitis bij allergische volwassenen.
- Door het gunstige veiligheidsprofiel wordt sublinguale immunotherapie aanbevolen bij kinderen met hooikoorts.
Wat is nieuw?
- Sublinguale immunotherapie is niet effectief om klachten van rhinoconjunctivitis te verminderen bij kinderen die bij de huisarts komen met hooikoorts.
- Ondanks het gunstige veiligheidsprofiel kan sublinguale immunotherapie vooralsnog niet worden aanbevolen voor de behandeling van hooikoorts bij kinderen.
Inleiding
De afgelopen jaren is sublinguale immunotherapie (SLIT) voorgesteld als een alternatief voor subcutane immunotherapie (SCIT). Dankzij de gemakkelijke toedieningsvorm en het goede veiligheidsprofiel, lijkt SLIT in het bijzonder geschikt voor kinderen.12 Recente meta-analyses gaven echter tegenstrijdige conclusies over de effectiviteit van SLIT bij kinderen.345 Het gunstige veiligheidsprofiel maakt SLIT ook geschikt voor gebruik in de eerste lijn. Het voorschrijven van immunotherapie door huisartsen heeft als bijkomend voordeel dat de introductie van immunotherapie plaatsvindt in een vroege fase van de ziekte, waardoor de ontwikkeling van astma en van nieuwe sensibilisaties mogelijk voorkomen wordt.67 Hoewel SLIT ideaal lijkt voor de behandeling van kinderen in de eerste lijn, zijn klinische trials met kinderen tot nu toe alleen uitgevoerd bij kinderen die zijn doorverwezen. Om de effectiviteit en veiligheid van SLIT te bepalen bij jongeren die bij de huisarts komen met een graspollengeïnduceerde allergische rhinoconjunctivitis, hebben wij een groot gerandomiseerd, dubbelblind, placebogecontroleerd onderzoek uitgevoerd.
Methoden
Voor een gedetailleerde beschrijving van de onderzoeksopzet verwijzen we naar het oorspronkelijke artikel.
Onderzoeksopzet
Geïncludeerde kinderen begonnen hun behandeling na afloop van het graspollenseizoen in september-oktober 2001 of in september-oktober 2002. Na afloop van het onderzoek (in respectievelijk 2003 en 2004) hebben we de gegevens samengevoegd. De Centrale Commissie Mensgebonden Onderzoek (CCMO) en de Medisch Ethische Toetsings Commissie van het Erasmus MC – Universitair Medisch Centrum gaven goedkeuring voor het onderzoeksprotocol. Alle deelnemers en hun ouders gaven schriftelijke toestemming.
Patiënten
Kinderen in de leeftijd van 6 tot 18 jaar met een ICPC-code R97 (hooikoorts/allergische rhinitis)8 werden door hun huisarts per brief uitgenodigd voor deelname en gescreend door een onderzoeksassistent. Inclusiecriteria waren IgE antilichamen voor graspollen = 0,7 kU/L, een voorgeschiedenis van rhinoconjunctivitis en een retrospectieve totale symptoomscore = 5. De kinderen scoorden retrospectief 5 symptomen (niezen, jeukende neus, waterige loopneus, neusobstructie en jeukende ogen) voor het voorgaande pollenseizoen (mei-augustus) op een schaal van 0-3 (0 = geen, 1 = mild, 2 = matig, 3 = ernstig; maximale totale score = 15). Exclusiecriteria waren het dagelijks gebruik van inhalatiecorticosteroïden gedurende = 3 maanden in het afgelopen jaar, immunotherapie in de afgelopen 3 jaar, sensibilisatie voor huisdieren aanwezig in het eigen huis (specifiek IgE = 0,7 kU/L), nasale aandoeningen die chirurgisch ingrijpen vereisen, en contra-indicaties voor immunotherapie.9 Verder bepaalden we IgE-antilichamen tegen huisstofmijt, berkpollen, en katten om mogelijke multisensibilisatie vast te stellen. Lage luchtwegsymptomen in de afgelopen twaalf maanden werden gemeten met de vragenlijst van de International Study of Asthma and Allergies in Childhood (ISAAC).10
Interventie
De verumbehandeling bevatte een mengsel van waterige extracten van vijf soorten graspollen (Lolium perenne, Phleum pratense, Dactylis glomeratein, Anthoxantum odoratum en Holcus lanatus) in een fosfaatbufferoplossing. De placebobehandeling bevatte alleen het oplosmiddel. Behandeling begon met een enkele druppel allergeen en werd verhoogd met een druppel per dag tot dag twintig. De onderhoudsdosis was twintig druppels twee keer per week, twee jaar lang. Naast schriftelijke instructies voor gebruik, kregen de deelnemers ook uitleg van een onderzoeksassistent. Een apotheker verdeelde de medicatie volgens een met de computer gegenereerde randomisatielijst, gestratificeerd voor symptoomscore (hoog versus laag) en huisarts. De deelnemers, hun ouders, onderzoekers en behandelende huisarts waren niet op de hoogte van de groepsindeling en konden geen onderscheid maken tussen verum- en placebobehandeling.
Uitkomstmaten
In de periode van mei tot en met augustus, na een en twee jaar behandeling noteerden de kinderen dagelijks de ernst van hun klachten, gebruik van symptoommedicatie en mogelijke bijwerkingen op een dagboekkaart. De symptomen niezen, jeukende neus, waterige loopneus, neusobstructie en jeukende ogen werden gescoord op een schaal van 0-3 (0 = geen, 1 = mild, 2 = matig, 3 = ernstig). Voor aanvang van het onderzoek besloten we alleen die dagen mee te tellen waarop er voldoende blootstelling aan graspollen was geweest.15 Secundaire uitkomstmaten waren het percentage symptoomvrije dagen, het percentage symptoommedicatievrije dagen, het type symptoommedicatie dat gebruikt werd, de ziektespecifieke kwaliteit van leven, de algemene indruk van behandeleffect, en de veiligheid. Aan het einde van het onderzoek waardeerden deelnemers en hun ouders het effect van de behandeling op een 6-punts schaal (1 = veel slechter, 2 = slechter, 3 = onveranderd, 4 = beter, 5 = veel beter, 6 = klachtenvrij). Het kind was therapietrouw wanneer de totaal ingenomen medicatie 80% van de voorgeschreven medicatie of meer bedroeg. Gedurende de tweejarige follow-up nam een onderzoeksassistent elke zes weken telefonisch contact op met de deelnemers. Van maart tot en met oktober werden de kinderen thuis bezocht.
Statistische analyse
De primaire uitkomstmaat was de gemiddelde dagelijkse totale symptoomscore gedurende de maanden mei tot en met augustus van het tweede behandeljaar. De steekproefomvang was gebaseerd op een eerder onderzoek onder volwassenen.13 Een verschil in primaire uitkomst tussen de behandelgroepen van ten minste 30% beschouwden we als het minimale klinisch relevante verschil.14 Om een verschil van 30% vast te stellen, waren 70 deelnemers in elke behandelgroep nodig (2-zijdige a = 0,05; power = 90%). Rekening houdend met mogelijke uitval stelden we als doel om 100 deelnemers in elke groep te randomiseren. Univariate analyse van de primaire uitkomst, van alle secundaire uitkomsten en therapietrouw analyseerden we met de Mann-Whitney-test of de χ2-test in het geval van percentages. Multivariate analyse voerden we uit met behulp van covariantieanalyse (ANCOVA) waarbij a-priori gedefinieerde covarianten werden geanalyseerd. Geslacht werd als niet geplande covariant toegevoegd, omdat de meisjes:jongens-ratio na randomisatie verschilde tussen de groepen. We hebben interactietermen onderzocht om na te gaan of baselinevariabelen het effect van de behandeling beïnvloedden. We hebben alle analyses uitgevoerd volgens het intention-to-treatprincipe. We hebben ook een per-protocolanalyse uitgevoerd, waarbij we deelnemers hebben uitgesloten die een incompleet of ontbrekend dagboek in het tweede jaar hadden en deelnemers die niet therapietrouw waren (dat wil zeggen met een medicatie-inname van < 80% van de voorgeschreven hoeveelheid). In alle analyses was p = 0,05 (2-zijdig) de grens voor statistische significantie.
Resultaten
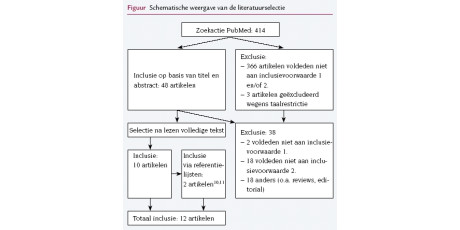
In 64 huisartsenpraktijken ontvingen 1590 kinderen een uitnodiging tot deelname aan het onderzoek. Er reageerden 829 (52%) kinderen, van wie er 384 aangaven niet geïnteresseerd te zijn. De belangrijkste reden om niet mee te doen was te weinig klachten (n = 117). Na toevoeging van nog 42 kinderen (29 uit een pilotonderzoek, en 13 broers of zussen), werden 487 kinderen gescreend (figuur 1). Tweehonderddrieëntachtig kinderen (58%) werden geëxcludeerd, vooral vanwege het dagelijks gebruik van inhalatiecorticosteroïden gedurende = 3 maanden in het voorafgaande jaar (n = 63) en IgE-antilichamen voor graspollen < 0,7 kU/L (n = 54). Uiteindelijk werden 204 kinderen gerandomiseerd voor behandeling met verum (n = 108) of placebo (n = 96). Alle deelnemers begonnen met de behandeling. Vijftig deelnemers (25%) beëindigden het tweejarige follow-uponderzoek voortijdig; van hen stopten 26 het onderzoek vóór het eerste graspollenseizoen. Tussen de behandelgroepen vonden we geen statistisch of klinisch significant verschil in het aantal vroegtijdig gestopte deelnemers en de redenen voor het vroegtijdig stoppen van het onderzoek. De belangrijkste reden om vroegtijdig te stoppen was het onvermogen om de onderzoeksmedicatie volgens schema in te nemen of om de dagboekkaart in te vullen (n = 31).
| Verum (n = 91) | Sd | Placebo (n = 77) | Sd | |
|---|---|---|---|---|
| Leeftijd (jaren) | 12,9 13,0 (7-17) | 2,6 | 12,5 13,0 (6-17) | 2,9 |
| Geslacht, aantal jongens | 61 (67%) | 34 (44%) | ||
| Retrospectieve symptoomscore | Gemiddelde 8,7 6,7 2,0 | Sd 2,6 2,2 0,8 | Gemiddelde 9,0 7,0 2,0 | Sd 2,4 2,1 0,9 |
| IgE graspollen, kU/L | Mediaan 75,8 | Range 0,8 tot 100 | Mediaan 76,8 | Range 1,6 tot 100 |
| Aantal deelnemers met multisensibilisatie | 69 | % 76 | 57 | % 74 |
| Aantal deelnemers met lage luchtwegsymptomen | 52 | 57 | 46 | 60 |
We hebben 168 kinderen geïncludeerd in de intention-to-treatanalyse (91 verum, 77 placebo). De kenmerken van deze populatie staan in tabel 1. De behandelgroepen waren vergelijkbaar voor wat betreft leeftijd, ernst van symptomen, specifiek IgE, multisensibilisatie en lage luchtwegsymptomen. Door toeval werden relatief meer jongens gerandomiseerd in de verumgroep. Dit gold zowel voor de in de intention-to-treat als de per-protocol populatie. We konden alle seizoenen analyseren, omdat de van tevoren vastgestelde limieten voor de graspollentelling werden behaald. Tijdens elk pollenseizoen van 123 dagen waren er 61 dagen met een pollentelling boven de mediaan. Een dagboekkaart konden we evalueren als tenminste 50% (dat wil zeggen 31) van deze dagen compleet waren ingevuld. Het gemiddeld aantal geëvalueerde dagen (standaarddeviatie, SD) was respectievelijk 55 (7) en 54 (8) dagen in de verum- en de placebogroep (p = 0,45).
| Verum (n = 91) | SEM | Placebo (n = 77) | SEM | P-waarde | |
|---|---|---|---|---|---|
| Gemiddelde totale dagelijkse symptoomscore (0-15) | 3,1 | 0,2 | 3,4 | 0,2 | 0,398 |
| Percentage symptoomvrije dagen (0-100) | 27,7 | 3,0 | 24,1 | 3,0 | 0,398 |
| Percentage symptoomverlichtende medicatievrije dagen (0-100) | 69,3 | 3,4 | 74,2 | 3,2 | 0,674 |
| Algehele evaluatie (1-6): | 3,9 3,7 | 0,1 0,1 | 3,8 3,7 | 0,1 0,1 | 0,143 0,643 |
| PRQLQ (6-11 jaar) Gemiddelde totaal score (0-6) | n = 30 1,7 | 0,2 | n = 26 1,4 | 0,1 | 0,799 |
| AdolRQLQ (12-17 jaar) Gemiddelde totaal score (0-6) | n = 56 1,7 | 0,2 | n = 47 2,1 | 0,2 | 0,272 |
De gemiddelde dagelijkse totale symptoomscore (standaarddeviatie) in de verumgroep was 3,1 (0,2) en 3,4 (0,2) in de placebogroep (p = 0,398; tabel 2). Covariantieanalyse (ANCOVA), met de vooraf gespecificeerde covariaten plus geslacht, voerden we uit met de primaire uitkomstmaat als afhankelijke variabele (tabel 3, totaalgroep). Het geadjusteerde verschil in gemiddelde totale dagelijkse symptoomscore was klein en bedroeg 0,1 op een schaal van 0 tot 15, in het voordeel van de verumgroep. De geadjusteerde gemiddelde totale dagelijkse symptoomscores bedroegen respectievelijk 3,2 en 3,3. De ratio van de beide gemiddelden (verum/placebo) bedroeg 0,97 (95%-BI 0,82-1,16). Alleen geslacht en retrospectieve totale symptoomscore hadden een significant effect op de uitkomstparameter.
| Totale groep – alle covariaten | Effect* | 95 %-BI | P-waarde | |
|---|---|---|---|---|
| Behandeling (verum minus placebo) | -0,08 | -0,66-0,50 | 0,778 | |
| Leeftijd (per jaar) | 0,01 | -0,10-0,11 | 0,927 | |
| Geslacht (vrouw minus man) | 0,76 | 0,17-1,35 | 0,012 | |
| Sensibilisatie voor huisstofmijt (ja minus nee) | -0,54 | -1,11-0,03 | 0,062 | |
| Sensibilisatie voor berkenpollen (ja minus nee) | 0,35 | -0,22-0,91 | 0,230 | |
| Retrospectieve totale symptoomscore (per punt) | 0,14 | 0,03-0,26 | 0,014 | |
| Leeftijd: | 36/38 55/39 | 0,12 -0,02 | -0,62-0,87 0,92-0,88 | 0,744 0,963 |
| Retrospectieve totale symptoomscore: | 47/38 44/39 | 0,03 -0,14 | -0,77-0,83 -1,05-0,76 | 0,934 0,756 |
Verdere analyse toonde dat geen enkele van de baselinevariabelen invloed had op het behandeleffect. Inclusie van de covarianten ‘jaar van inclusie’ en ‘gebruik van nasale corticosteroïden in de maand voorafgaand aan het geëvalueerde seizoen’ (3 verum, 5 placebo) had geen effect op de uitkomst. De subgroepanalyses naar leeftijd en retrospectieve totale symptoomscore lieten evenmin een verschil zien (tabel 3, subgroepen). Analyse per-protocol toonde ook geen significant verschil in symptoomscore tussen de beide behandelgroepen. Tussen de beide behandelgroepen was er geen statistisch significant verschil in het percentage therapietrouwe patiënten (80% [73/91] verum versus 71% [55/77] placebo; p = 0,312). Zoals te zien in figuur 2 volgen de symptoomscores en de pollentellingen elkaar in beide behandelgroepen. Onderzoeksdagen van het tweede jaar deelden we in aan de hand van de dagelijkse pollentelling (3) en we bepaalden in elke categorie de gemiddelde totale dagelijkse symptoomscore voor iedere deelnemer. Figuur 3 laat zien dat een stijging van de gemiddelde totale dagelijkse symptoomscore correleert met het aantal pollen. Binnen de verschillende pollentellingscategorieën vonden we geen significante verschillen tussen de behandelgroepen (voor alle vier: p = 0,30). Ook de analyses van de secundaire uitkomstmaten (weergegeven in tabel 2) toonden geen statistisch significante verschillen tussen de behandelgroepen.
Er was geen significant verschil in het totaal aantal dagen waarop symptoommedicatie werd gebruikt. Analyse van de soorten symptoommedicatie liet geen verschillen zien tussen de verumgroep en de placebogroep wat betreft het gemiddelde percentage van dagen waarop cetirizine (18,9% versus 17,2%), levocabastine oogdruppels (8,6% versus 6,9%) en nasale corticosteroïden (6,0% versus 4,0%) werden gebruikt. Alleen het gebruik van xylometazoline verschilde significant tussen de groepen (verum 3,4% versus placebo 5,9% van de dagen; p = 0,022). Van de mogelijke bijwerkingen zagen we alleen lokale orofaryngeale reacties vaker in de verumgroep (verum 39% versus placebo 17% van de deelnemers; p = 0,001). Deze reacties waren mild. Systemische anafylactische reacties kwamen niet voor.
Discussie
Op dit moment is dit het grootste onderzoek met SLIT bij kinderen en het eerste onderzoek dat is uitgevoerd in de eerste lijn. We toonden aan dat SLIT met graspollen, toegepast in de eerste lijn, niet beter is dan placebo om symptomen en medicatiegebruik te reduceren bij kinderen met rhinoconjunctivitis. Eerdere onderzoeken werden uitgevoerd bij kinderen die doorverwezen waren, de resultaten van deze relatief kleine en heterogene onderzoeken zijn tegenstrijdig.16171819202122232425 In ons onderzoek vonden we op geen enkele uitkomstmaat een effect van SLIT. Wij berekenden dat de maximaal te verwachten reductie in symptoomscores 18% is, aanzienlijk minder dan de minimale klinisch relevant geachte verbetering van 30%.14 Bij de interpretatie van onze resultaten zijn enkele kanttekeningen op zijn plaats. De eerste kanttekening is of, gezien de mogelijk minder ernstige klachten in de eerste lijn, eventuele effectiviteit wel zou kunnen worden aangetoond bij deze patiënten. Behalve de retrospectieve symptoomscore hebben we geen indicatie van de ernst van de symptomen voor aanvang van het onderzoek. De retrospectieve symptoomscore geeft mogelijk een overschatting van de ernst van de symptomen. Gegevens over kwaliteit van leven tijdens het onderzoek tonen echter aan dat de kinderen praktische problemen en dagelijkse hinder ondervonden van hun klachten, zodat er tenminste sprake is van matige rhinitis, terwijl het percentage dagen met symptomen (verum 72% en placebo 76%) aangeeft dat er sprake is van persisterende rhinitis.26 Dergelijke patiënten zijn volgens de ARIA-richtlijnen goede kandidaten voor immunotherapie.26 Twee grote onderzoeken stelden bovendien vast dat ongeveer 90% van de patiënten die bij de huisarts kwam matige tot ernstige rhinitis heeft.2728 Bodtger et al. toonden aan dat hoewel een retrospectieve post-seizoenevaluatie op een 4-punts schaal de ernst van de symptomen overschatte, deze evaluatie goed gebruikt kon worden als basis voor randomisatie.29 Wij konden een overschattingseffect uitsluiten, omdat er ook bij kinderen met een retrospectieve totale symptoomscore hoger dan de mediaan geen significant behandeleffect was. Multi-gesensibiliseerde patiënten hebben mogelijk minder baat bij specifieke immunotherapie dan monogesensibiliseerde patiënten.28 In ons onderzoek includeerden we zowel mono- als multigesensibiliseerde patiënten. Ongeveer 75% van de kinderen waren multigesensibiliseerd, wat waarschijnlijk representatief is voor de gemiddelde allergische populatie bij huisarts en specialist. Analyse van alleen de monogesensibiliseerde patiënten toonden geen significant verschil tussen de verumgroep en de placebogroep (gegevens niet weergegeven). Ook de multivariate analyse (ANCOVA) liet geen effect van co-sensibilisatie zien. Symptomen fluctueerden met de mate van blootstelling, maar zelfs op dagen met een hoge blootstelling en dus hogere symptoomscores vonden we geen significant verschil tussen de behandelgroepen. Het is onwaarschijnlijk dat symptoommedicatie en met name nasale steroïden de effectiviteit hebben gemaskeerd, omdat het gebruik beperkt was en gelijkmatig verdeeld over de groepen. In overeenstemming met het protocol voerden we ook een analyse uit waarop we alle dagen meerekenden, onafhankelijk van de pollentelling (gegevens niet weergegeven). Ook bij deze analyse vonden wij geen effect van SLIT op symptoomscore en medicatiegebruik. Een van de grote voordelen van SLIT is het gunstige veiligheidsprofiel. In ons onderzoek vonden we slechts milde bijwerkingen in beide behandelgroepen. De verumgroep meldde significant meer lokale reacties in de orofaryngeale holte. Een onderzoek onder volwassenen die geïncludeerd waren via huisartsenpraktijken vond frequente maar goed te verdragen bijwerkingen en concludeerde dat SLIT veilig is in de algemene populatie.30 Gegevens over de therapietrouw bij SLIT zijn schaars.1617182324 De therapietrouw in ons onderzoek was goed. Het is mogelijk dat deze in de dagelijkse praktijk, als patiënten niet zo intensief worden begeleid, minder is. De optimale therapeutische dosis is nog altijd niet vastgesteld. De grote verscheidenheid aan gebruikte allergeenpreparaten en gebrek aan informatie over de dosering maken het moeilijk om onderzoeken onderling te vergelijken. In het huidige onderzoek bedroeg de totale dosis 4,5 mg equivalent Lolium perenne pollen (Lol p 5) gegeven gedurende 24 maanden. We kunnen niet uitsluiten dat een hogere dosis zou kunnen leiden tot een beter resultaat. Een recent onderzoek naar SLIT met graspollen bij volwassenen suggereerde een dosisgerelateerde respons. Behandeling met de hoogste dosis van 1,9 mg equivalent Phleum pratense pollen (Phl p 5) gegeven gedurende 4,5 maanden leidde echter niet tot een klinisch relevante verlaging van symptoomscores.31 Samenvattend concluderen we dat SLIT met graspollen niet effectief is bij jongeren met seizoensgebonden allergische rhinoconjunctivitis. Op grond hiervan kan SLIT niet worden aanbevolen aan huisartsen als behandeling voor kinderen of adolescenten met graspollenallergie.
Reacties
Er zijn nog geen reacties.